重医研制、我国首个获批上市化学发光法新冠病毒抗体检测试剂盒研制的背后
科技日报消息,抗体检测3日被《新型冠状病毒肺炎诊疗方案(试行第七版)》纳入新冠肺炎的确诊依据,重庆研发制造的抗体检测试剂盒已正式上市。
3月4日,重庆市科技局发布消息,重庆市抗新型冠状病毒重点应急攻关研究项目,成功研发出新冠病毒IgM/IgG抗体检测试剂盒,已于3月1日通过国家药品监管局应急审批,获准上市,成为我国首个获批上市的化学发光法新冠病毒抗体检测产品。
抗体检测可独立或与核酸检测相互印证,减少错诊、漏诊。该项目由重庆医科大学牵头联合博奥赛斯(重庆)生物科技有限公司研发,产学研携手紧急攻关不断让新的检测手段满足临床一线需要。
发布会现场。科技日报记者 雍黎摄
抗体检测首次被纳入确诊依据
钟南山院士曾发出呼吁,希望 IgM 试剂盒能尽快通过。呼吁的就是抗体检测,这是国家卫健委首次将抗体检测纳入确诊依据。
为什么会被纳入确诊依据?
项目负责人,中华医学会微生物学与免疫学分会主任委员,重庆医科大学感染性疾病分子生物学教育部重点实验室执行主任黄爱龙解释,病毒入侵人体后,人体免疫系统中的效应B细胞会分泌产生与病原微生物结合的免疫球蛋白,就是通常说的“抗体”。无论是正在被病毒感染的患者,还是曾经感染过病毒、现已治愈的人,在体内都可以检测到抗体。
与核酸检测需要获取患者的带病毒咽拭子、鼻拭子等标本不同,抗体检测取材于静脉血,用血清进行检测,因此也属于血清学检测,血液中的病毒含量相对来说比较低,可以降低被感染的风险,对医护人员更加安全。
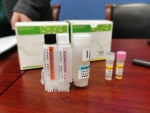
发布会现场展示的新冠病毒IgM/IgG抗体检测试剂盒。科技日报记者 雍黎摄
检测更安全更快更便宜
此次重庆医科大学牵头研制的两种新冠病毒IgM/IgG抗体检测试剂盒,是我国首个获批上市的化学发光法新冠病毒抗体检测产品,具有检测方式安全、检测快速、高通量、低成本等诸多优势。
该项检测采用全自动流水线设备进行,可以实现快速、大量检测,首报告时间为30分钟,最快检测速度可达每小时400人份,且成本较低。
截至2月26日,该抗体试剂盒已在重庆、湖北累计完成13532例样本测试,其中1362例新冠确诊病例,结果显示IgM灵敏度为93.7%,特异性为99.4%;IgG灵敏度为89.6%,特异性为99.2%。
黄爱龙解释,特异性是将实际无病的人正确地判定为真阴性的比例,简单讲,就是正确地判定无病者的能力。灵敏度则是将实际有病的人正确地判定为真阳性的比例,简单讲,就是衡量某种技术检测出有病者的能力。
据了解,该试剂盒已经实现量产,产量可达20万人份/周,目前已经储备100万人份的量。
研发团队在实验室工作。重庆医科大学供图
优中选难
确定攻关研究主攻方向
疫情发生后,重庆医科大学研究团队在第一时间开展论证并启动了试剂盒研发工作。1月22日研究团队确定了应急攻关研究的主攻方向——基于化学发光的新型冠状病毒IgM/IgG的免疫诊断试剂。
“当时抗体免疫诊断试剂还是空缺。”该项目负责人黄爱龙教授说,病原体的检测分为直接针对病原体的检测和抗体免疫检测,病毒学诊断需要进行核酸诊断和血清学免疫诊断进行配合。疫情发生后,核酸检测国内已经有企业可以提供,不过免疫诊断试剂还是空缺。
免疫学主要有胶体金和化学发光等检测方式。胶体金检测使用方便快速,所有反应能在15分钟内完成,成本低、应用范围广,但也存在灵敏度低、无法定量、采用血液有暴露风险等不足。化学发光免疫分析是比较可靠的体外免疫诊断技术之一,检测灵敏度高,更简便、更安全、通量高、速度快、时间短,不过有较高的技术门槛,国内具有研发能力的单位不多。
“我们实验室是感染性疾病分子生物学教育部重点实验室,一直从事肝炎病毒的研究,有基础,而博奥赛斯生物科技有限公司擅长化学发光检测。”黄爱龙说,他们一拍即合,立即联合重庆派金生物科技有限公司,发挥各自优势,组建团队开展了产学研联合应急科技攻关。
重庆医科大学负责抗原抗体设计与制备和临床实验,博奥赛斯生物科技有限公司负责试剂盒组装、产品报批和批量生产。
国家药监局官网截图
大胆设计小心验证
5天找到抗体
当时学校已经开始放假,实验室不少老师和学生已经离开重庆,内部发起紧急攻关号召后,留在重庆的老师学生立即组织了起来。
“5天!差不多5天左右做出来的,我们每天只睡了不到5个小时。”在重庆医科大学感染性疾病分子生物学教育部重点实验室里,汪德强教授谈起当时的情形依然记忆犹新。他和蔡雪飞老师带领着6个博士研究生负责抗原抗体设计制备,这是整个项目的基础也是最难的一部分。
做抗体检测首先就需要找到抗体,但新冠病毒体外表达是一种未知表达,哪些蛋白质会产生抗原性,需要做蛋白结构解析,然后进行预测、设计,再合成验证。汪德强说,“我们当时设计了两条路径,一是根据SARS的研究报道反推可能会产生免疫性的蛋白质,第二路径是根据公布的病毒基因序列进行抗原表位肽设计合成。”就像拆定时炸弹,预测的对不对,在验证“剪线”前谁也不知道。
“如果不对就前功尽弃!”蔡雪飞说,在正常情况下验证一个需要5-7天,但当时他们加急到48小时,如果验证不对就要重新再做。幸运的是他们一次就成功了,而且找到的6个抗原蛋白中3个都有效,且效果是最好的。“这里面离不开汪教授的专业判断和经验。”
不计成本
各方携手只为一个目标
从1月23日首批抗原表位肽设计合成,到27日完成重组抗原的设计与密码子优化,28日准备制备重组抗原制备的前期工作。
“当时研发上是争分夺秒,费用上是不计成本。”汪德强说,疫情发生时临近春节,人和物都差,而且面临交通难题。差人,能回学校的老师学生积极请战;差设备、原料,学校就组织各个学院紧急支援。
为避免实验失败,全部采取两个组同时独立推进,一个人加样,一个人检查复核。因为重庆没有验证制备需要的生物技术服务类公司,合作方博奥赛斯努力克服各种困难提供制备服务。为提高原核表达的效率,项目组对设计的6个重组抗原进行密码子优化需要基因合成,在上海负责基因合成的上海生工安排专人制作。物流交通已停,他们安排专人乘飞机取送,而且采用接力的形式,负责专人不出机场,只往返于重庆、天津、上海三地的机场护送。
黄爱龙说:“疫情紧急,人命关天!这次我们和合作方都是不讲成本,不说困难,只为了一个目标——尽快把检测试剂盒做出来!”
项目团队临床验证工作。重庆医科大学供图
临床验证马不停蹄
“老婆等着我们检测盒!”
产品初步研发成功后,团队马不停蹄开展验证工作。
“当时还是有些忐忑,毕竟到一线面临着被感染的风险。”陈娟说,不过试剂盒和后期的优化改进都少不了要过临床的验证这一关,这是关键。为了避免家人被传染,组里的几位成员都统一住进了学校的宿舍。她5岁的儿子知道妈妈是去找打败病毒的方法,也懂事地没有哭闹,每天通话都鼓励她:“妈妈,加油!”
“我是老党员,又是学医的,有风险的地方让我来!”从一开始就组织协调各方事宜的科研处处长袁军,冲锋在前,七下万州深入疫区定点医院病房,协调工作,收集转运标本,五上歌乐山公共卫生救治中心洽谈业务,亲自驾车装运标本,两赴永川医院转运标本样品和材料,足足一个月没有回家,行程接近5000公里。他坚信,早出科技成果,就可能挽救更多的病人,保护更多的医护人员不受病毒感染。
“老婆在前方等着我们的试剂盒。”副研究员龙泉鑫心中还有一份牵挂。他除夕夜从海南赶回投入研究攻关,而妻子钱克莉是一名感染科医生,作为重庆援助湖北医疗队的一员,正在武汉市中心医院支援。他说,“老婆知道并支持自己的研究,期待着呢。”
“很高兴,我们的研究成果通过审批上市!目标实现了!”黄爱龙表示,这是我们基础科研支撑临床的一次紧急大练兵,也是产学研合作的有力成果。短短一个月能够从研发到上市,离不开各界的支持,感动的事很多、感谢的话很多,但他知道不必说,因为大家的目标都是一个——齐心协力抗击新冠。
科技日报记者 雍黎
原标题:我国首个获批上市化学发光法新冠病毒抗体检测试剂盒研制的背后
【免责声明】上游新闻客户端未标有“来源:上游新闻-重庆晨报”或“上游新闻LOGO、水印的文字、图片、音频视频等稿件均为转载稿。如转载稿涉及版权等问题,请与上游新闻联系。